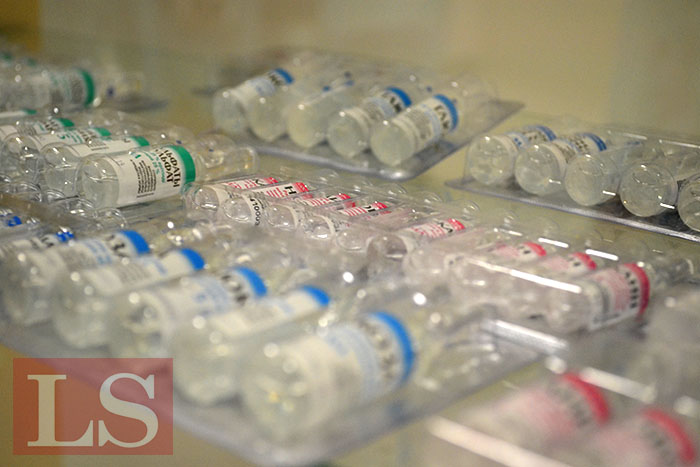
В Евразийском экономическом союзе (ЕАЭС) утвержден список актов в сфере обращения лекарственных средств, которые разработают в ближайшие два года, сообщает LS со ссылкой на Евразийскую экономическую комиссию (ЕЭК).
Отмечается, что в 2016-2018 годах планируется разработать 67 документов по вопросам регулирования общего рынка лекарственных средств в рамках ЕАЭС. Перечень утвержден членом коллегии по техническому регулированию ЕЭК Валерием Корешковым. За каждым государством будет закреплена разработка определенного списка актов.
Документы будут охватывать регулирование обращения лекарственных средств по трем группам вопросов: производство и качество, требования к лекарственным препаратам альтернативной медицины и доклиническое и клиническое изучение лекарственных средств.
Первыми будут разработаны в 2016 году три проекта - руководства по валидации процесса производства лекарственных препаратов, требования к воде, используемой для производства лекарственных средств, требования к исследованию стабильности лекарственных препаратов и фармацевтических субстанций. Варианты уже представлены белорусскими разработчиками во II квартале 2016 года и обсуждаются рабочей группой.
На предстоящем заседании рабочей группы по лекарственным средствам в Алматы, которое состоится 25-26 августа, должны быть рассмотрены разработанные Казахстаном проекты руководства по подготовке досье лекарственных препаратов (плацебо, активный контроль) для клинических исследований и требований к показателям качества лекарственных препаратов с модифицированным высвобождением для приема внутрь.